Детская эпилептология (разина е.е.)
Содержание:
- Несколько слов об «эпи»-признаках и заключении ЭЭГ.
- Особенности клинических проявлений эпилепсии в зависимости от локализации патологического очага
- Диагностика фокальной эпилепсии
- Аффективно-респираторный синдром: МКБ, классификация
- Образец бланка для интерпретации ЭЭГ
- К каким докторам следует обращаться если у Вас Детская эпилепсия с пароксизмальной активностью на ЭЭГ в затылочной области:
- Общие принципы лечения эпилепсии
- Характеристика эпилептиформной активности
- Симптомы Детской эпилепсии с пароксизмальной активностью на ЭЭГ в затылочной области:
- Классификация ЭЭГ по Людерс
- Прогнозы и лечение Аффективно-респираторного синдрома
- Эпилепсия: причины возникновения заболевания
- ПОНЯТИЕ ЭПИЛЕПСИИ
- Классификация ЭЭГ по Gibbs
- Синдром Леннокса-Гасто.
Несколько слов об «эпи»-признаках и заключении ЭЭГ.
Стандартное заключение ЭЭГ многословно, в нем подробно описываются особенности режима функционирования головного мозга. Большая часть описываемых изменений всего лишь нейрофизиологические особенности Вашего организма в данный момент времени и не требуют какой-либо лечебной коррекции, иными словами и с «легкими» и с «умеренными диффузными изменениями» на ЭЭГ люди живут долго и счастливо. Как правило ЭЭГ заключение должна завершать фраза о наличии или отсутствии «очаговых (локальных)» и «пароксизмальных» изменений/нарушений. Строго говоря и то и другое нормой не являются, но и каким-либо «однозначным приговором» никогда не были, наличие в описании ЭЭГ очаговых или пароксизмальных изменений мотивация посетить врача-невролога, который уже на основании ЭЭГ, других исследований и собственного диагностического мышления подскажет какой лечебной тактики надо придерживаться в каждом конкретном случае.
Даже при наличии типичных – как на картинке в учебнике – ЭЭГ изменений патогномоничных для эпилептических нарушений врач функциональной диагностики не имеет право поставить диагноз эпилепсия. Мало того, нередко за эпилептические пароксизмальные изменения принимают то, что к эпи-активности не имеет никакого отношения – например высокочастотную активность в бета-диапазоне (15 и более Гц). Подобный вид активности описывается как явление ирритации (по-русски: раздражение) и свидетельствует о высоком уровне возбуждения в коре. Он может быть признаком, к примеру, депрессивного расстройства, но никак не свидетельствует в пользу эпилепсии.
Ниже приведены «яркие» примеры пароксизмальных изменений эпилептического характера.

Нестойкая паркосизмальная активность — по типу «острые волны-медленные волны», искаженная, спровоцирована фотостимуляцией.

А вот такую активность можно назвать стойкой пароксизмальной и добавить «эпиформного характера», волны настолько высокие что на иллюстрации масштаб уменьшен в два раза.

У того же пациента «цифровая достройка» пространственной локализации очага патологической активности с помощью программы BrainLoc 6.0 (программа пространственной локализации источников патологической активности в структурах головного мозга)
Важно отметить что по сравнению с теми методами диагностики которые оказывают побочное «вредное» воздействие на организм – такие как рентген, МРТ, КТ — снятие биопотенциалов с поверхности тела человека при проведении ЭЭГ, ЭКГ – оказывает на самого человека не больше воздействия чем работающий рядом компьютер
Особенности клинических проявлений эпилепсии в зависимости от локализации патологического очага
Височная форма фокальной эпилепсия является самой часто встречаемой. Эпилептогенный очаг расположен в височной доле головного мозга. Височная фокальная эпилепсия характеризуется припадками с потерей сознания, наличием автоматизмов и ауры. Приступ длится в среднем 30-60 секунд. Оральные автоматизмы присущи детям, а автоматизмы по типу жестов – взрослым. Пароксизмы височной фокальной эпилепсии имеют вторничную генерализацию. Постприступная афазия фиксируется при поражении доминантного полушария височной доли головного мозга.
Эпилептический очаг лобной фокальной эпилепсии расположен в лобной доле головного мозга. Данный очаг провоцирует кратковременные пароксизмы, которые могут проходить сериями. Для лобной ФЭ не характерна аура. Симптомы лобной ФЭ: поворот глаз и головы в одну сторону, сложные автоматические жесты, эмоциональное возбуждение, крики, вздрагивания, агрессия. Если очаг патологии находится в предцентральной извилине, то появляются двигательные пароксизмы джексоновской эпилепсии. Эпилептические приступы лобной фокальной эпилепсии возникают во время сна.
При расположении очага в затылочной доле головного мозга происходят эпилептические приступы, сопровождающиеся нарушением зрения. Например, сужение зрительных полей, зрительные галлюцинации, иктальное моргание, транзиторный амавроз и др. Длительность зрительных галлюцинаций – 13 минут.
Расположение очага эпилептической активности в теменной доле является редкостью. Теменная доля поражается в случае наличия опухоля или корковой дисплазии. Теменная фокальная эпилепсия характеризуется простыми соматосенсорными пароксизмами: кратковременная афазия или паралич Тодда. Если зона эпилептической активности локализуется в постцентральной извилине, то могут происходить джексоновские припадки.
Диагностика фокальной эпилепсии
Если парциальный пароксизм возник впервые, то пациенту необходимо детальное обследование, так как данный симптом может быть проявлением серьезной церебральной патологии. Во время консультации врач-невролог просит полностью описать длительность, характер, последовательность развития эпилептического приступа. Выявленные отклонения помогают установить расположение очага патологии.
Эпилептическая активность диагностируется с помощью ЭЭГ. Эпи-активность фокальной эпилепсии можно зафиксировать на ЭЭГ даже в межприступный период. Если ЭЭГ без приступа малоинформативна, то следует провести электроэнцефалоскопию с провокационными пробами и/или во время приступа. Субдуральная кортикография – это электроэнцефалоскопия с установлением электродов под твердой мозговой оболочкой. Помогает точно определить локализацию патологического очага.
Из инструментальных методов исследований наиболее эффективным для выяснения морфологических основ ФЭ является МРТ. Толщина срезов должна составлять около 1-2 мм, чтобы как можно точнее обнаружить мельчайшие дефекты вещества головного мозга. В случае симптоматической эпилепсии МРТ даёт возможность выявить первопричину: очаговые поражения, атрофии, дисплазии. В ряде случаев обнаружить подобные изменения не удается и тогда диагноз — идиопатическая или криптогенная ФЭ. В качестве дополнительного, но необязательного исследования может быть назначена ПЭТ головного мозга. ПЭТ зафиксирует эпилептогенный участок как зону повышенной метаболической активности. ОФЭКТ также применяется в качестве дополнительного метода диагностики, в ходе которого специалист способен отслеживать динамику перфузии церебрального вещества: в течение припадка будет наблюдаться картина гиперперфузии эпилептогенного очага, а в отрезок времени между пароксизмами — гипоперфузия.
Аффективно-респираторный синдром: МКБ, классификация
- Легкая стадия. Длится около 15 секунд, ребёнок не способен нормально дышать. Опасности для мозга нет, но всё равно стоит обратиться к неврологу.
- «Бледная» стадия. Возникает из-за внешних факторов. Например, из-за боли, удара, укола или падения. При приступах, у ребёнка наблюдается бледность, он может упасть в обморок. Аффективные симптомы типа плача или крика могут не проявляться.
- «Синяя» стадия. Катализатором приступов является окружающая обстановка: стресс, давление, сильное возбуждение. Симптомами при этой стадии являются: кожа становится синей, апноэ длится около 20 секунд, в редких случаях проявляются судороги.
- Осложнённый Аффективно-респираторный синдром. Часто проявляется у грудничков. Данная стадия отличается от прошлых своей сложностью и длительностью приступов. Синдром проявляется не только из-за темперамента или характерных особенностей, но и из-за проблем с ЦНС.
Образец бланка для интерпретации ЭЭГ
Компьютерное ЭЭГ-обследование
Дата обследования_
Фамилия, имя, отчество_возраст_диагноз_
Общая характеристика электрической активности
1. Организована. 2. Дезорганизована. 3. Гиперсинхронна. 4. Уплощена. 5. Учащена. 6. Замедлена.
-
α-Ритм
- Частота: 7-8, 9-11, 11-13 Гц, неустойчивая.
- Регулярность: регулярен, нерегулярен, в виде групп волн, отсутствует. По данным спектрального анализа ЭЭГ индекс α составляет: амплитуда: снижена, повышена, нормальна; зональные различия: сохранены, снижены; форма α-волны: синусоидальная, заостренная, аркообразная, слабо модулированная.
- Межполушарная асимметрия: нет, слабая, отчетливая.
- β-Активность: частота, амплитуда, локализация, индекс.
- θ-Активность: частота, амплитуда, локализация, индекс.
- δ-Активность: частота, амплитуда, локализация, индекс.
- Пароксизмальная активность: острые волны и пики, множественные пароксизмы, пик-волна, билатер. синхр. вспышки-α, θ, δ.
Функциональные пробы
- Реакция активации (проба с открыванием глаз): реакция отсутствует, слабая, выраженная, провокация пароксизмальной активности или иной патологической активности.
- Гипервентиляция:не изменяет, усиливает α-, θ-, δ-актив., нарастание дизритмии, синхронные пароксизмы θ или δ, генерализованные разряды, локальные пик-волны
- Ритмическая фотостимуляция: депрессия, РУР в узком, широком диапазоне низких, высоких частот, межпол. асим., провоцирование эпи-разрядов.
- Звуковые раздражения:реакция нормальна, усилена, ослаблена
На основании картирования спектров мощности ЭЭГ выявлено: локальные проявления: неотчетливые, асимметрия, преобладание, фокус, очаг;
- топография: правая, левая, асимметрия затылочная, теменная, центральная, лобная, височная;
- стволовые знаки: незначительные, умеренные, выраженные, срединные, передние отделы.
К каким докторам следует обращаться если у Вас Детская эпилепсия с пароксизмальной активностью на ЭЭГ в затылочной области:
Невролог
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Детской эпилепсии с пароксизмальной активностью на ЭЭГ в затылочной области, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору – клиника Eurolab всегда к Вашим услугам! Лучшие врачи осмотрят Вас, изучат внешние признаки и помогут определить болезнь по симптомам, проконсультируют Вас и окажут необходимую помощь и поставят диагноз. Вы также можете вызвать врача на дом. Клиника Eurolab открыта для Вас круглосуточно.
Как обратиться в клинику:
Телефон нашей клиники в Киеве: (+38 044) 206-20-00 (многоканальный). Секретарь клиники подберет Вам удобный день и час визита к врачу. Наши координаты и схема проезда указаны здесь. Посмотрите детальнее о всех услугах клиники на ее персональной странице.
Общие принципы лечения эпилепсии
В настоящее время выработаны общепринятые международные стандарты по лечению эпилепсии, которые необходимо соблюдать для повышения эффективности лечения и улучшения качества жизни пациентов.
Лечение эпилепсии может быть начато только после установления точного диагноза. Термины “предэпилепсия” и “профилактическое лечение эпилепсии” являются абсурдными. Существуют две категории пароксизмальных неврологических расстройств: эпилептические и неэпилептические (обмороки, снохождения, ночные страхи и пр.), и назначение АЭП оправдано только в случае эпилепсии. По мнению большинства неврологов, лечение эпилепсии следует начинать после повторного приступа. Единичный пароксизм может быть “случайным”, обусловленным лихорадкой, перегревом, интоксикацией, метаболическими расстройствами и не относиться к эпилепсии. В этом случае немедленное назначение АЭП не может быть оправданным, так как данные препараты являются потенциально высокотоксичными и не применяются с целью “профилактики”. Таким образом, АЭП могут применяться только в случае повторных непровоцируемых эпилептических приступов (т.е. при эпилепсии по определению).
В случае установления точного диагноза эпилепсии необходимо решить вопрос, следует или нет назначать АЭП? Разумеется, в подавляющем большинстве случаев, АЭП назначаются немедленно после диагностирования эпилепсии. Однако при некоторых доброкачественных эпилептических синдромах детского возраста (прежде всего, при роландической эпилепсии) и рефлекторных формах эпилепсии (эпилепсия чтения, первичная фотосенситивная эпилепсия и др.), допускается ведение пациентов без применения АЭП. Подобные случаи должны быть строго аргументированы.
Диагноз эпилепсии установлен и решено назначить АЭП. С 1980-х годов в клинической эпилептологии прочно утвердился принцип монотерапии: купирование эпилептических приступов должно осуществляться преимущественно одним препаратом. С появлением хроматографических методов определения уровня АЭП в крови стало очевидным, что многие антиконвульсанты имеют взаимный антагонизм, и одновременное их применение может значительно ослабить противосудорожный эффект каждого. Кроме того, применение монотерапии позволяет избежать возникновения тяжелых побочных эффектов и тератогенного воздействия, частота которых значительно возрастает при назначении нескольких препаратов одновременно. Таким образом, в настоящее время полностью доказана несостоятельность старой концепции о назначении большого количества АЭП одновременно в малых дозах. Политерапия оправдана только в случае резистентных форм эпилепсии и не более 3-х АЭП одновременно.
Подбор АЭП не должен быть эмпирическим. АЭП назначаются строго в соответствии с формой эпилепсии и характером приступов. Успех лечения эпилепсии во многом определяется точностью синдромологической диагностики (табл. 3).
АЭП назначаются, начиная с малой дозы, с постепенным увеличением до достижения терапевтической эффективности или появления первых признаков побочных эффектов. При этом определяющим является клиническая эффективность и переносимость препарата, а не содержание его в крови (табл. 4).
В случае неэффективности одного препарата, он должен быть постепенно заменен другим АЭП, эффективным при данной форме эпилепсии. При неэффективности одного АЭП нельзя сразу прибавлять к нему второй препарат, то есть переходить на политерапию не используя всех резервов монотерапии.
Принципы отмены АЭП.
АЭП могут быть отменены спустя 2,5-4 года полного отсутствия приступов. Клинический критерий (отсутствие приступов) является основным критерием отмены терапии. При большинстве идиопатических форм эпилепсии отмена препаратов может осуществляться через 2,5 (роландическая эпилепсия) — 3 года ремиссии. При тяжелых резистентных формах (синдром Леннокса-Гасто, симптоматическая парциальная эпилепсия), а также при юношеской миоклонической эпилепсии, данный период увеличивается до 3-4 лет. При продолжительности полной терапевтической ремиссии в течение 4-х лет, лечение должно быть отменено во всех случаях. Наличие патологических изменений на ЭЭГ или пубертатный период пациентов не являются факторами, задерживающими отмену АЭП при отсутствии приступов более 4-х лет.
Не существует единого мнения по вопросу о тактике отмены АЭП. Лечение может быть отменено постепенно в течение 1-6 мес или одномоментно по усмотрению врача.
часть-1 часть-2
Характеристика эпилептиформной активности
Для количественной и объективной оценки ЭЭГ каждый графоэлемент может быть описан рядом параметров: типом, амплитудным максимумом, симметричностью, продолжительностью и др.
➥Более подробно: Визуальные характеристики ЭЭГ
Типы разрядов
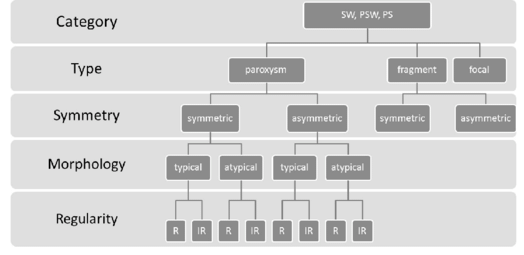 Иерархическая классификация эпилептиформных разрядов
Иерархическая классификация эпилептиформных разрядов
SW = комплекс спайк-волна, PSW = комплекс полиспайк-волна, PS = полиспайк, R = регулярные, IR = нерегулярные
Эпилептиформная активность классифицируется по длительности на:
- фрагменты (длительность <2 с)
- пароксизмы (длительность ≥2 с)
Бифронтальные разряды (как симметричные, так и асимметричные) относятся к фрагментам фронтальной экспрессии генерализованной эпилептиформной активности и не классифицируются как очаговые.
Амплитудный максимум
Амплитуда волны измеряется от пика до пика и выражается в микровольтах. Когда максимальная амплитуда осциллограммы зашкаливает в отведениях F3, F4 и Fz, она маркируется как фронто-центральный максимум. Аналогично, Fp1, F3, Fp2, F4 и O1, O2 определяются как фронто-полярные и затылочные максимумы соответственно.
Амплитудная симметрия
Канал ЭЭГ, показывающий максимальную амплитуду эпилептиформных разрядов, берется за эталон и сравнивается с тем же каналом в противоположном полушарии. Более 50% разницы амплитуд между полушариями принимается за амплитудную асимметрию.
Регулярность пароксизмов
Генерализованные пароксизмы определяются как нерегулярные, когда вместо регулярных ритмических иктальных разрядов имеются медленные волны или комплексы различной частоты и/или морфологии, или короткие (<1 с), кратковременные прерывания судорожных приступов.
Морфология
Классический отрицательный пик/-ки, сопровождаемый куполообразной волной, основанный на визуальном анализе, рассматривался как типичная морфология. Волны без спайков и спайков поверх волны считаются нетипичными. Когда ≥50% разрядов пароксизма имеют аномальную морфологию, он классифицировался как пароксизм аномальной морфологии.
Фотопароксизмальный ответ
Генерализованные спайко-волновые, полиспайк-волновые и/или полиспайковые разряды, вызванные прерывистой фотостимуляцией, определяются как фотопароксизмальный ответ (PPR). Когда PPR сохраняется после окончания стимуляции дольше чем 100 мс, его классифицируют как незатухающий. PPR мoжет отражать идиопатические, генетически детерминированные признаки, которые появляются на ЭЭГ при отсутствии эпилептических приступов.
Чувствительность к закрытию глаз
Чувствительность к закрытию глаз определяли как эпилептиформные разряды, появляющиеся в течение 1–3 с после закрытия глаз и продолжающиеся 1–4 с, но не в течение всего периода с закрытыми глазами.
Симптомы Детской эпилепсии с пароксизмальной активностью на ЭЭГ в затылочной области:
Возраст начала вариабелен (15 мес. — 17 лет). Пик манифестации симптомов 5-7 лет.
- Приступы и дебют имеют 2 различных варианта:
- 1. Ранний дебют (2-7 лет). Редкие ночные приступы, начинающиеся со рвоты, девиации глаз в сторону и нарушением сознания. Иногда — переход в гемиконвульсивный или генерализованный тонико-клонический приступ.
- 2. Поздний дебют (старше 7 лет). Преходящие нарушения зрения — 65%, амавроз — 52%, элементарные зрительные галлюцинации — 50%, сценоподобные галлюцинации — 14%. Сознание чаще сохранено, приступы, как правило, в дневное время. Гемиклонические судороги — 43%, ГКТП — 13%, автоматизмы — 13%, версивные движения — 25%. Послеприступное состояние в 33% случаев сопровождается головной, чаще мигренеподобной болью, в 17% — тошнотой и рвотой. Провоцирующие факторы: в 25% — резкая смена освещенности при переходе из темного помещения в светлое.
Психика обычно без особенностей, иногда — эмоциональные расстройства. В нейропсихологическом статусе — снижение зрительной памяти, проявления идеомоторной апраксии.
Неврология, как правило, без особенностей.
Классификация ЭЭГ по Людерс
Классификация ЭЭГ по Людерс очень детальна, она включает как артефакты, так и редко встречающиеся типы ЭЭГ.
- Медленная активность
- Замедление фоновой активности
- Преходящее замедление
- Продолженное замедление
- Эпилептиформные паттерны
- Спайки
- Острые волны
- Доброкачественные эпилептические разряды детства BEDC
- Комплексы спайк-волна
- Медленные комплексы спайк-волна
- 3-Гц комплексы спайк-волна
- Полиспайки
- Гипсаритмия
- Фотопароксизмальный ответ
- ЭЭГ паттерн приступа
- ЭЭГ паттерн статуса
- ЭЭГ со сплошными артефактами
- Специальные паттерны
- Избыточная быстрая активность- excessive fast activity
- Асимметрия
- Начало сна с БДГ
- Периодический паттерн
- Трифазные волны
- Периодические латерализованные эпилептиформные разряды (PLEDs)
- Паттерн вспышка-подавление
- Угнетение фоновой активности
- Паттерны комы
- Альфа-кома
- Веретенная кома
- Бета-кома
- Тета-кома
- Дельта-кома
- Электроцеребральная инактивность
- Нормальные варианты и неспецифические паттерны ЭЭГ
- Височное замедление у пожилых
- Затылочные дельта волны у подростков
- Глоссокинетический артефакт
- Лобные тета (“ритм Циганека”)
- Медленная активность при гипервентиляции FIRDA
- Вариант медленного фонового альфа-ритма
- Лямбда-волны
- Позитивные затылочные острые компоненты сна POSTS
- Доброкачественные эпилептиформные феномены во сне – малые острые спайки
- Wicket-спайки
- 6-Гц позитивные спайки
- Вертексные волны
- “Спайки” rectus lateralis
- 6-Гц “фантомные” спайк-волны
- Медленная активность при гипервентиляции
- 14- и 6-Гц позитивные спайки
- Телефонный артефакт
- Усвоение ритма фотостимуляции
- Ритмические тета волны в дремоте (психомоторный вариант)
- Субклинические эпилептиформные ритмические разряды у взрослых SREDA
- Гипнагогическая гиперсинхрония
- Глазные движения
- Двигательный артефакт
- ЭКГ артефакт
Прогнозы и лечение Аффективно-респираторного синдрома
Какие могут быть осложнения:
- Эпилепсия;
- Гипоксия;
- Проблемы с памятью;
- Растерянность;
- Расстройство в мыслительных действиях;
- Проблемы с речью.
Чтобы сократить количество и сложность приступов у детей, опытные неврологи советуют наблюдаться у психотерапевта и на регулярной основе проходить лёгкую реабилитацию в клиниках:
- Песочной терапией;
- Микротоком;
- Сенсорной интеграцией;
- Нейропсихологической коррекцией.
При возникновение даже неочевидных симптомов подобного расстройства, следует обращаться к специалистам в целях предотвращения развития заболевания. Нужно понимать, что первая стадия с возрастом может развиться, что сильно затруднит лечение. Если находиться на постоянном наблюдение у врачей и следовать всем рекомендациям, с аффективно-респираторным синдромом можно жить спокойно.
Эпилепсия: причины возникновения заболевания
Причины, приводящие к формированию эпилептического очага, разнообразны, ведущими среди них являются органические поражения мозга и наследственное отягощение. Развитие методов нейровизуализации позволило расширить и углубить представления об органической основе эпилепсии. Исследования с помощью методов компъютерной томографии (КТ), магнитно-резонансной томографии (МРТ), позитронно-эмиссионной томографии (ПЭТ) позволили выявить у значительного числа больных эпилепсией структурные изменения головного мозга. В детском возрасте они чаще всего являются следствием перинатальных повреждений мозга (гипоксии, инфекций, родовой травмы), врожденных пороков развития мозга. У взрослых основное значение приобретает повреждение мозга в связи с:
- черепно-мозговыми травмами,
- инфекциями центральной нервной системы,
- метаболическими расстройствами,
- токсическими факторами.
При эпилепсии пожилых людей главными факторами риска являются цереброваскулярные заболевания и опухоли головного мозга. Случаи, когда установлены наличие органического поражения головного мозга и его причина, относят к симптоматической эпилепсии. К криптогенной эпилепсии относят те клинические наблюдения, когда удается выявить поражение мозга, но причина его остается неизвестной. В большинстве случаев эпилепсии никакой причинной связи заболевания с конкретной патологией выявить не удается (идиопатическая эпилепсия). В развитии этой формы эпилепсии большое значение придают генетической отягощенности.
По мнению ученых, по наследству передается не сама болезнь, а предрасположенность к ней, обусловленная определенными биохимическими изменениями вещества мозга, повышающими его «судорожную готовность». Наследственно обусловленная предрасположенность к судорогам может проявиться при неблагоприятных условиях: врожденных пороках развития, болезнях матери во время беременности, родовых травмах, различных инфекционных заболеваниях, травмах раннего периода детства. Согласно современным представлениям, эпилепсию обусловливает комбинация наследственных и средовых факторов.
Значимость различных этиологических факторов заболевания существенно изменяется с возрастом. Так, в детском возрасте чаще встречаются генетически обусловленные формы эпилепсии, у взрослых наблюдается значительное превалирование симптоматических эпилепсий, в развитии которых генетические факторы не имеют решающего значения.
ПОНЯТИЕ ЭПИЛЕПСИИ
ЭПИЛЕПСИЯ — хроническое заболевание головного мозга, характеризующееся повторными приступами,
которые возникают в результате чрезмерной нейронной активности и сопровождаются различными
клиническими и параклиническими проявлениями. В основе эпилепсии лежит повышенная нейронная
активность с высоковольтными гиперсинхронными разрядами (эпилептический очаг). Наиболее часто
эпилептические приступы встречаются в детском возрасте. Приступы у детей характеризуются
не только высокой частотой, но и большей степенью выраженности. Именно в период,
когда идет интенсивное развитие мозга, приступы могут привести
к вторичным изменениям со стороны психики ребенка. Отсюда становится ясным
необходимость наиболее ранней специализированной медицинской и социальной помощи таким
детям. К сожалению, общество негативно настроено к людям с эпилептическими приступами
и их проблемам, что выражается в словах, обычно употребляемых по отношению к ним: — «припадок»,
«припадочный» , «эпилептик», а также существованию целого ряда неоправданных социальных
ограничений. Эти проблемы довольно успешно решаются в мире. В большинстве стран
имеются региональные организации общественного или государственно-общественного типа, занимающиеся вопросами
социальной помощи людям с эпилептическими приступами. У детей различные судорожные
состояния встречаются в 5-10 раз чаще, чем у взрослых, что, очевидно, связано
с особенностями строения и функции головного мозга, с напряженностью и несовершенством регуляции
метаболизма, лабильностью и тенденцией к иррадиации возбуждения, с повышенной проницаемостью сосудов,
гидрофильностью мозга и пр. В происхождении эпилепсии основное значение имеет взаимодействие
наследственной предрасположенности и поражения головного мозга. При большинстве форм эпилепсии
отмечается полигенная наследственность, причем в одних случаях она имеет большую,
в других — меньшую значимость. При анализе наследственности нужно учитывать прежде
всего явные признаки болезни, придавая определенное значение и таким
ее проявлениям, как заикание, учитывать характерологические особенности личности (конфликтность, злобность,
педантизм, назойливость). К предрасполагающим факторам относятся органические церебральные дефекты
перинатального или приобретенного (после нейроинфекций или черепно-мозговой травмы) характера.
Патогенез эпилепсии включает ряд механизмов.
Это прежде всего фокальность, которая характерна не только для парциальной эпилепсии,
но и для первично генерализованных приступов. Наиболее часто генерализованные приступы возникают
при очаговых поражениях медиобазальной височной и орбитофронтальной локализации. По мере прогрессирования
заболевания формируется эпилептическая система и процесс распространяется на весь мозг.
Биохимические механизмы эпилепсии связаны с расстройством ионных, медиаторных и энергетических
процессов, Так, ионные сдвиги ведут к повышению мембранной проницаемости
и усилению в результате этого деполяризации нейронов, их сверхвозбудимости. Снижение запасов
глюкозы и накопление молочной кислоты в ткани головного мозга во время
приступа являются причиной ацидотических сдвигов; усугубляющих гипоксию и снижающих
уровень фосфатных соединений. Перед приступом часто обнаруживается метаболический
алкалоз. Имеют значение и иммунологические реакции с образованием при повторных приступах
противомозговых антител, циркуляторные расстройства и другие факторы, расширяющие зону
поражения. Специфических патологоанатомических изменений при эпилепсии не находят. Вместе с тем эпилептический
процесс может вызывать тяжелые дистрофические изменения и уменьшение количества
ганглиозных клеток, прогрессирующий глиоз, особенно — в височных долях. Клиническая
картина эпилепсии у детей имеет некоторые характерные особенности. К ним можно
отнести полиморфизм и возрастную трансформацию приступов, высокий удельный вес,
частоту абортивных форм, наличие синдромов, не встречающихся у взрослых, нередкое
развитие послеприступных симптомов очагового поражения мозга.
Классификация ЭЭГ по Gibbs
По данным Gibbs и др. (1943), нормальная ЭЭГ представлена:
- записями, в которых доминируют альфа-волны и имеется небольшое число быстрых и медленных волн,
- записями, в которых доминируют низкой амплитуды быстрые колебания, смешивающиеся с низкоамплитудной активностью (ниже 20 мкВ) различной частоты.
Пользуясь этими критериями, Gibbs и др. записали нормальную ЭЭГ у 85–90 % обследованных здоровых взрослых людей. Greenstein и др. (1948) считают, что при оценке «нормальности» ЭЭГ существенное значение имеет и так называемый дельта-индекс. Он не должен превышать 8 в лобном отведении (по отношению к ушному электроду) и 5 – в других отведениях. Кроме того, быстрая активность, если она появляется симметрично в обоих полушариях и не отдельными вспышками, даже если она диффузно не распространена по коре больших полушарий головного мозга, не должна рассматриваться как отклонение от нормы.
Синдром Леннокса-Гасто.
Синдром Леннокса-Гасто (СЛГ) – эпилептическая энцефалопатия детского возраста, характеризующаяся полиморфизмом приступов, специфическими изменениями ЭЭГ и резистентностью к терапии. Частота СЛГ составляет 3-5% среди всех эпилептических синдромов у детей и подростков; болеют чаще мальчики.
Заболевание дебютирует, преимущественно, в возрасте 2-8 лет (чаще 4-6 лет). Если СЛГ развивается при трансформации из синдрома Веста, то возможно 2 варианта:
Инфантильные спазмы трансформируются в тонические приступы при отсутствии латентного периода и плавно переходят в СЛГ.
Инфантильные спазмы исчезают; психомоторное развитие ребенка несколько улучшается; картина ЭЭГ постепенно нормализуется. Затем спустя некоторый латентный промежуток времени, который варьирует у разных больных, появляются приступы внезапных падений, атипичные абсансы и нарастает диффузная медленная пик-волновая активность на ЭЭГ.
Для СЛГ характерна триада приступов: пароксизмы падений (атонически- и миоклонически-астатические); тонические приступы и атипичные абсансы. Наиболее типичны приступы внезапных падений, обусловленные тоническими, миоклоническими или атоническими (негативный миоклонус) пароксизмами. Сознание может быть сохранено или выключается кратковременно. После падения не наблюдается судорог, и ребенок сразу же встает. Частые приступы падений приводят к тяжелой травматизации и инвалидизации больных.
Тонические приступы бывают аксиальными, проксимальными или тотальными; симметричными либо четко латерализованными. Приступы включают в себя внезапное сгибание шеи и туловища, подъем рук в состоянии полуфлексии или разгибания, разгибание ног, сокращение лицевой мускулатуры, вращательные движения глазных яблок, апноэ, гиперемию лица. Они могут возникать, как в дневное время, так и особенно часто, ночью.
Атипичные абсансы также характерны для СЛГ. Проявления их многообразны. Нарушение сознания бывает неполным. Может сохраняться некоторая степень двигательной и речевой активности. Наблюдается гипомимия, слюнотечение; миоклонии век, рта; атонические феномены (голова падает на грудь, рот приоткрыт). Атипичные абсансы обычно сопровождаются понижением мышечного тонуса, что вызывает как бы “обмякание” тела, начиная с мышц лица и шеи.
В неврологическом статусе отмечаются проявления пирамидной недостаточности, координаторные нарушения. Характерно снижение интеллекта, не достигающее, однако, тяжелой степени. Интеллектуальный дефицит констатируется с раннего возраста, предшествуя заболеванию (симптоматические формы) или развивается сразу после появления приступов (криптогенные формы).
При ЭЭГ-исследовании в большом проценте случаев выявляется нерегулярная диффузная, часто с амплитудной асимметрией, медленная пик-волновая активность с частотой 1,5-2,5 Гц в период бодрствования и быстрые ритмические разряды с частотой около 10 Гц – во время сна.
При нейровизуализации могут иметь место различные структурные нарушения в коре головного мозга, включая пороки развития: гипоплазия мозолистого тела, гемимегалэнцефалия, кортикальные дисплазии и пр.
В лечении СЛГ следует избегать препаратов, подавляющих когнитивные функции (барбитураты). Наиболее часто при СЛГ применяются вальпроаты, карбамазепин, бензодиазепины и ламиктал. Лечение начинается с производных вальпроевой кислоты, постепенно увеличивая их до максимально переносимой дозы (70-100 мг/кг/сут и выше). Карбамазепин эффективен при тонических приступах – 15-30 мг/кг/сут, но может учащать абсансы и миоклонические пароксизмы. Ряд больных реагирует на увеличение дозы карбамазепина парадоксальным учащением приступов. Бензодиазепины оказывают эффект при всех типах приступов, однако этот эффект временный. В группе бензодиазепинов применяются клоназепам, клобазам (фризиум) и нитразепам (радедорм). При атипичных абсансах может быть эффективен суксилеп (но не как монотерапия). Показана высокая эффективность комбинации вальпроатов с ламикталом (2-5 мг/кг/сут и выше). В США широко используется комбинация вальпроатов с фелбаматом (талокса).
Прогноз при СЛГ тяжелый. Стойкий контроль над приступами достигается лишь у 10-20% больных. Прогностически благоприятно преобладание миоклонических приступов и отсутствие грубых структурных изменений в мозге; негативные факторы – доминирование тонических приступов и грубый интеллектуальный дефицит.